【天坛-紫金·药物政策云沙龙(十一)】罕见病多方共治模式的中国探索
发布日期:2023-03-06来源:中国药品监督管理研究会
2月27日晚,由中国药品监督管理研究会药品监管法规和政策研究专业委员会、中国药品监督管理研究会药品监管人才培养研究专业委员会、中国药科大学药品监管科学研究院、国家药品监督管理局药品监管创新与评价重点实验室、江苏省药学会药事管理专业委员会联合主办,中国药科大学国家药物政策与医药产业经济研究中心(NDPE)承办的【天坛-紫金·药物政策云沙龙】第十一期活动“罕见病多方共治模式的中国探索”在线上成功举办。

图1 天坛-紫金药物政策云沙龙(第十一期)活动主题
本期云沙龙专家报告环节由中国药科大学药品监管科学研究院常务副院长茅宁莹教授主持,互动研讨环节由研究院席晓宇特聘研究员主持。会议首先由中国药品监督管理研究会张伟会长致辞。张会长指出,罕见病诊疗及保障水平的提升需要中国医学工作者、临床药学工作者以及政策研究者的不断努力,探索出破解罕见病防治难题的“中国模式”。专家报告分别由苏州诺景生命科技有限公司郑维义董事长、中国医学科学院血液病医院血液学研究所张磊副所院长、蔻德罕见病中心(CORD)创始人黄如方主任带来《孤儿药研发的中国实践》《临床医生参与罕见病药物研发的经验分享》《患者组织如何推动罕见病药物研发》专题分享,南京医科大学附属儿童医院张爱华院在互动研讨环节分享了精彩观点。
会议中,郑维义董事长基于我国罕见病药物研发现状,从科学技术、伦理规范以及支付体系三方面重点阐述了孤儿药研发亟待解决的关键问题,并指出中国孤儿药研发应采取面向全球市场的国际化开发策略,将成为中国创新药走向世界的捷径。来自中国医学科学院血液病医院血液学研究所的张磊副所院长,作为罕见病多方共治体系中的医疗机构主体代表,以研究者发起的临床试验为主题,分享了血液病医院临床研究整体的发展模式以及细胞和基因治疗研究与转化现状,并以国内首个批准进入临床试验的血友病基因治疗药物为例,对探索高效、多中心临床研究模式展开了详细阐述;最后张院长指出未来数据科学与医学研究的有机结合,形成大规模、高质量的前瞻性队列,突破临床试验难点推动医学研究创新,助力探索构建研究型医院的中国模式。最后,蔻德罕见病中心(CORD)创始人黄如方主任代表罕见病患者组织,分享了对推动罕见病药物研发的思考。黄主任从患者的专业性、资金力量、行业研发能力及环境、行业的偏见四个方面分析了中国患者组织缺席罕见病创新药研发的问题,并指出亟需政府及基金会的介入和推动促进患者组织全流程参与到罕见病药物研发全过程,发挥患者组织在多元共治体系中的应有作用。
互动研讨中,南京医科大学附属儿童医院张爱华院长认为,罕见病药物研发难度大,需要临床医务人员、医疗机构、医药企业和社会各界人士等多方主体合作推进,包括罕见病诊疗体系建设,药物的研发以及罕见病医疗保障政策的完善等领域。郑维义董事长谈到,罕见病药物立项研发要走国际化道路,选择临床急需的产品,并以患者为中心,以临床价值为导向进行开发研究。中国药科大学药品监管科学研究院常务副院长茅宁莹教授指出,罕见病患者的诊疗是一个病有所医,医有所药,药有所保,保有所得的整体性支撑体系;多主体,多部门需要一个整体的协同机制来联动,实现罕见病防治与保障体系多元主体的共治共享。
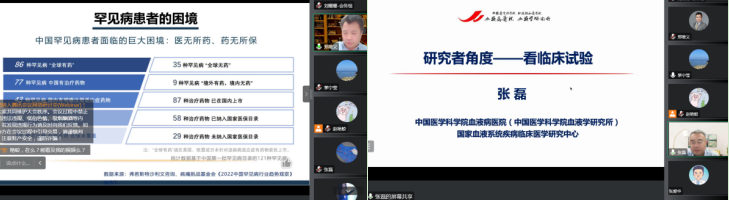
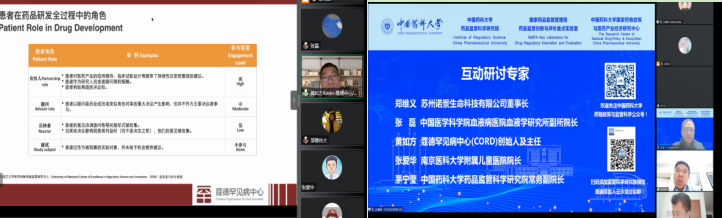
图2 专家报告分享
作为今年的第一期活动,本期活动受到医药行业各领域的关注和参与。罕见病药物的研发离不开临床医疗机构、医药企业和社会各界人士的共同推进和努力,更需要政策法规的科学指引。【天坛-紫金·药物政策云沙龙】活动举办至今,努力整合政策制定、推行、研究和实践方面的专家,本期活动围绕着罕见病诊疗、药物研发和患者组织的权益等热点、焦点和难点问题进行了深入研讨,共同推进罕见病防治与保障事业迈上新的台阶。
本站由中国药品监督管理研究会主办 版权所有 未经许可禁止转载或建立镜像
Copyright © CNCSDR All Rights Reserved
备案序号:京ICP备14043040号
中国药品监督管理研究会信息中心建设和维护
地址:北京市东城区 | 邮编:100050
