国家药监局委托课题系列报道 ▏2022年度研究会立项课题结题会
发布日期:2023-01-06来源:中国药品监督管理研究会
《国内外药品技术指导原则体系对比研究》
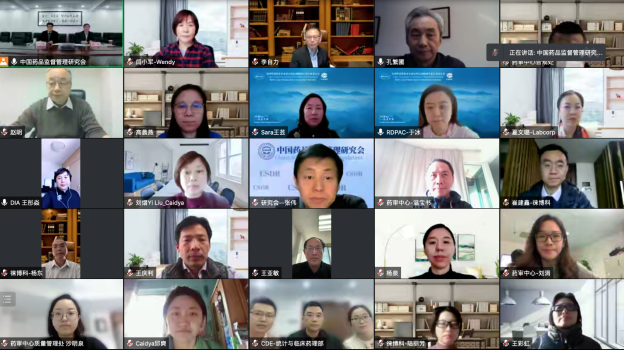
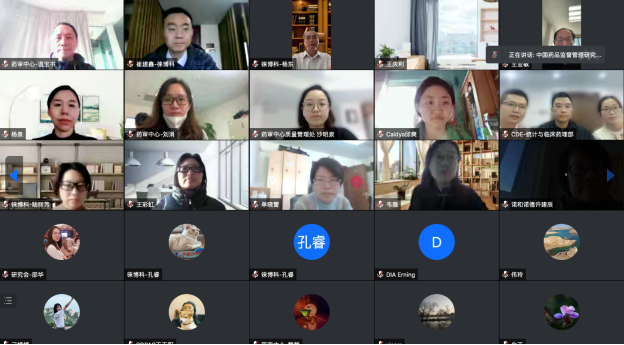
2022年12月28日,受国家药品监督管理局药品审评中心(CDE)委托,由中国药品监督管理研究会立项并由药品研究监管国际交流专业委员会承接的“国内外药品技术指导原则体系对比研究”结题会,以线上线下相结合的方式召开。国家药监局药品审评中心孔繁圃主任、中国药品监督管理研究会张伟会长,药审中心质量管理处及各审评相关部门负责人及工作人员出席了会议。会议由中国药品监督管理研究会副会长兼秘书长时立强主持。
会上,研究会药品监管研究国际交流专业委员会薛斌主任委员汇报了课题结题情况。四个工作小组负责人杨泉(RDPAC)、杨东(徕博科)、崔建鑫(徕博科)和刘熠(DIA)分别就药学、非临床药理毒理、临床药理及临床专业的具体内容进行了汇报。
药审中心领导、质量管理处及各个审评部门各位专家听取了课题汇报,充分肯定了课题的研究成果和现实意义,专家一致认为课题研究根据行业需求,全面评估了境内外技术指导原则对比现状。对今后制定适合中国国情的药品技术指导原则,提供了详实的理论依据。专家组对课题研究报告提出了部分意见。
张伟表示,感谢药审中心领导和各部门对课题研究工作的支持,在课题研究过程中多次召开沟通交流会,全程互动、精准对接。课题组在清晰明确的目标下,重点关注我国行业核心问题,通过对比和分析中外技术指导原则存在的差异和原因,对后续我国技术指导原则制修订及培训工作提出相关建议。并表示研究会将结合课题研究成果中培训需求,积极搭建培训平台,提高培训评估效果,争取在2023年为行业提供更多的服务。
孔繁圃指出2023年是全面贯彻落实党的20大精神的开局之年,我国监管部门坚持以人民为中心,以监管和行业热点难点为导向,积极推进药品审评标准体系建设,本次委托研究会开展的“国内外药品技术指导原则体系对比研究课题”,全面评估国了内外药品研究技术指导原则的比对情况,对进一步完善我国技术指导原则的体系建设,推动药品审评标准与国际化接轨有着非常重要的意义。后续药审中心将分批推动课题成果的实际转化,为推动我国医药产业创新发展贡献力量。
《中国医疗器械关键核心技术和关键零配件现状调研2期》
2022年12月30日,由国家药品监督管理局立项,中国药品研究会承担,《中国医疗设备》杂志社、首都医科大学生物医学工程学院共同牵头开展研究的“中国医疗器械关键核心技术和关键零配件现状调研2期”课题结题会于线上顺利召开。
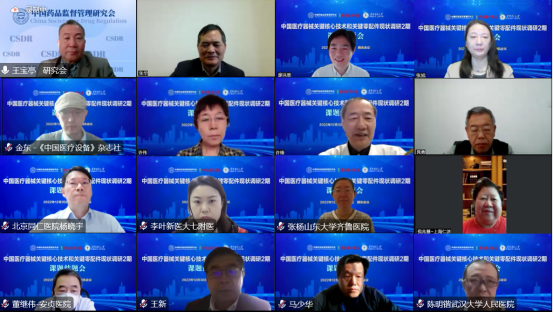
课题评审专家清华大学医学院廖洪恩副院长、国家药品监督管理局医疗器械注册管理司张华副司长、北京大学第三医院北方院区许锋副院长、中国人民解放军总医院医疗保障中心晁勇副主任、中国药品监督管理研究会王宝亭副会长、国家药品监督管理局医疗器械技术审评中心原副主任许伟教授出席会议。廖洪恩副院长担任课题评审专家组组长。课题负责人《中国医疗设备》杂志社金东社长、首都医科大学张旭教授以及课题组各产品线专家再线参加了本次会议。会议由张旭教授主持。

会上,课题组负责人金东代表课题组向专家组汇报了“中国医疗器械关键核心技术和关键零配件现状调研2期”的研究情况。
评审专家就课题组汇报的内容进行了充分讨论,肯定了课题的成果和价值。该课题针对我国部分高端医疗器械及其关键核心技术和关键零配件发展现状深入一线开展调研,通过“中国医疗设备行业数据研究员”调研体系和“医疗器械关键核心技术专家库”资源,以及“好医工App”信息平台收集的大量数据,开展了超声、监护、检验设备、口腔设备、麻醉、腔镜、血透、DSA、放疗、核医学、康复共11条产品线的关键核心技术和关键零配件分析研究。为了该课题研究,在行业中遴选出了高水平专家并组成了专业研究团队,建立了先进的数据分析模型,形成了科学的研究体系。该课题研究分析了我国上述类别医疗器械存在的诸多技术难点问题,并为政府进一步制定、完善相关医疗器械管理政策提供了科学依据及建议,对推动我国高端医疗器械健康发展,解决高端医疗器械“卡脖子”问题,明确部分高端医疗器械科技攻关方向,促进高端医疗器械研发生产,保障国家医疗安全和人民群众的生命健康提供有效数据支撑及决策参考。

最后,王宝亭副会长对课题的成果表示充分肯定。认为该课题为进一步明确我国高端医疗器械“卡脖子”问题所在提供了重要依据。这对于政府相关部门规划、支持我国医疗器械行业发展具有重大意义。建议继续深入该课题研究,逐步形成“我国高端医疗器械关键核心技术及关键零配件发展现状资料库”,为我国医疗器械行业发展贡献力量。
本站由中国药品监督管理研究会主办 版权所有 未经许可禁止转载或建立镜像
Copyright © CNCSDR All Rights Reserved
备案序号:京ICP备14043040号
中国药品监督管理研究会信息中心建设和维护
地址:北京市东城区 | 邮编:100050
