“紫金药物政策云沙龙——美国制药企业药物警戒实操经验分享会”成功举办
发布日期:2022-02-08来源:中国药品监督管理研究会
1月20日,由中国药品监督管理研究会药品监管法规和政策研究专业委员会、江苏省药学会药事管理专业委员会、中国药科大学药品监管科学研究院、国家药品监督管理局药品监管创新与评价重点实验室联合主办,中国药科大学国家药物政策与医药产业经济研究中心(NDPE)承办的“美国制药企业药物警戒实操经验分享会”——紫金药物政策云沙龙第二期活动在腾讯会议线上成功举办,张伟会长线上参加会议。
中国药科大学药品监管科学研究院常务副院长茅宁莹教授担任大会主席、由中国药科大学药品监管科学研究院药物警戒专家委员会秘书柳鹏程副教授主持会议。百济神州(美国)药物警戒总监Joseph Cardullo先生和高级经理Jean Ohara女士两人相互配合,从美国药物警戒法规体系、检查协调、PV检查重点关注问题、PV检查步骤、483表格和最终检查结论、检查结果分类、检查回应等方面做了详细介绍,并分别以辅以案例进行深入讨论与点对点剖析。在随后的讨论互动环节,中国药科大学药品监管科学研究院药物警戒专家委员会委员、百济神州药物警戒高级总监张轶菁女士与Joseph Cardullo先生和Jean Ohara女士一同围绕美国药物警戒检查相关知识与恒瑞医药等企业线上代表进行了深入热烈的探讨。
本次研讨会受到了行业的高度关注和积极参与,来自国家药品监督管理局药品监督管理司、国家药品监督管理局食品药品审核查验中心、国家药品监督管理局药品审评中心、上海药品审评核查中心、江苏省药品监督管理局审评中心、甘肃省药品和医疗器械不良反应监测中心等监管机构代表,清华大学、郑州大学、南京医科大学、南京中医药大学、沈阳药科大学等医药高校代表,江苏省中西医结合医院、上海长海医院等医疗机构代表,中国医药创新促进会、上海市食品药品安全研究会等行业协会代表,恒瑞医药、贝达药业等企业代表,累计300余人同时参与并互动讨论。今后,紫金药物政策云沙龙系列还将继续聚焦行业热点,为行业搭建沟通交流平台,为政府及其有关部门建言献策。
图1 紫金药物政策云沙龙(第二期)线上会场
图2 Joseph Cardullo先生作深入解读
图3 Jean Ohara女士作深入解读
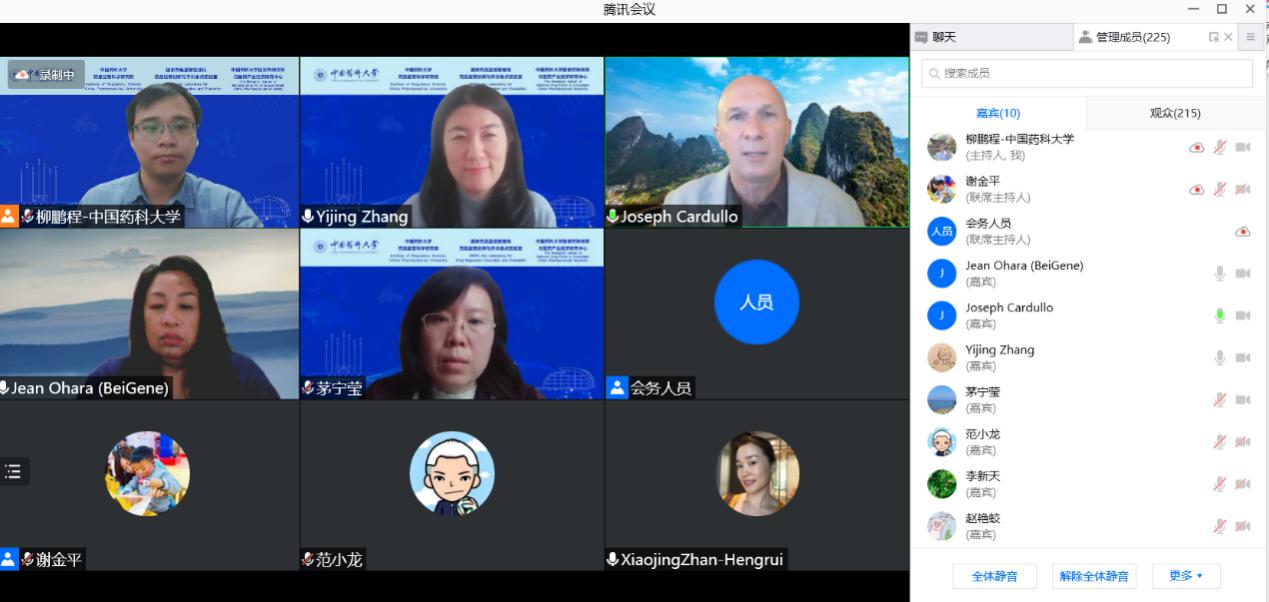
图4与会嘉宾与观众互动研讨
本站由中国药品监督管理研究会主办 版权所有 未经许可禁止转载或建立镜像
Copyright © CNCSDR All Rights Reserved
备案序号:京ICP备14043040号
中国药品监督管理研究会信息中心建设和维护
地址:北京市东城区 | 邮编:100050
